Las moléculas diatómicas son moléculas formadas por dos átomos unidos químicamente.

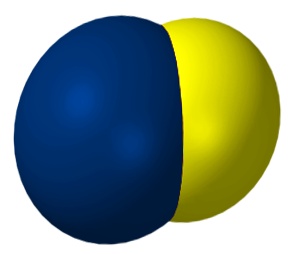
Los átomos pueden ser del mismo elemento (moléculas homonucleares), o de elementos diferentes (moléculas heteronucleares).
Ejemplos familiares de moléculas diatómicas de elementos son los cinco elementos diatómicos en estado gaseoso: Cl2, F2 H2, N2,y O2.
En total, se conocen siete elementos diatómicos a temperatura ambiente; los otros son el Br2 (líquido) y el I2 (sólido).
Ejemplos familiares de moléculas diatómicas que contienen elementos diferentes son el cloruro de hidrógeno (HCl), el monóxido de carbono (CO) y el monóxido de nitrógeno (NO).
Enlace en moléculas diatómicas
En las moléculas diatómicas homonucleares, el enlace es covalente.Cada átomo de la molécula tiene igual electronegatividad; los electrones se comparten por igual entre los dos átomos.
En las moléculas diatómicas heteronucleares, los átomos difieren en electronegatividad; estas moléculas tienen enlaces covalentes polares.La molécula forma un dipolo.
Algunos compuestos tienen fórmulas que podrían sugerir que son moléculas diatómicas, como el NaCl.De hecho, en lugar de compartir electrones para formar moléculas, el cloruro de sodio es un producto de la ionización.En condiciones normales, los compuestos iónicos no forman moléculas diatómicas.En condiciones normales, los compuestos iónicos no forman moléculas diatómicas. A temperatura ambiente, la mayoría existen como grandes redes de iones dispuestas en redes cristalinas.Por ejemplo, en el caso del cloruro de sodio sólido, cada ion está rodeado por seis iones de carga opuesta en una enorme red de iones.
En la fase gaseosa, sin embargo, el NaCl puede existir como una molécula diatómica con un enlace covalente polar.