Acido salicilico Proprietà chimiche, usi, produzione
Materiali sintetici organici importanti
L’acido salicilico è una materia prima sintetica organica importante, ampiamente usata in medicina, pesticidi, coloranti, gomma, cibo e profumi. Nell’industria farmaceutica, le principali produzioni di droga dell’acido salicilico sono salicilato di sodio, olio di wintergreen (salicilato di metile), aspirina (acido acetilsalicilico), ammina di acido salicilico, salicilato di fenile. Nell’industria dei coloranti, viene utilizzato per la produzione di mordente giallo puro, giallo diretto 3GN, giallo diretto GR, marrone diretto 3GN, marrone mordente acido G, giallo mordente acido GG, giallo acido complesso colorante. Nella produzione di pesticidi, l’acido salicilico è usato per la sintesi del pesticida organico al fosforo Isocarbophos, intermedio isopropilico salicilato isofenphos metile e rodenticida warfarin, intermedio coumatetralyl 4-hydroxycoumarin. Nell’industria della gomma, è usato come agente anti-scottatura e produzione di assorbente ultravioletto e agente schiumogeno. È materiale di profumo, utilizzato per la preparazione di salicilato di metile, estere etilico dell’acido salicilico; conservanti alimentari, il suo sale di sodio è per lo più utilizzato, ora un certo numero di paesi sono stati vietati; salicilato di metile può essere utilizzato come agenti di pulizia orale, come il sapore del dentifricio.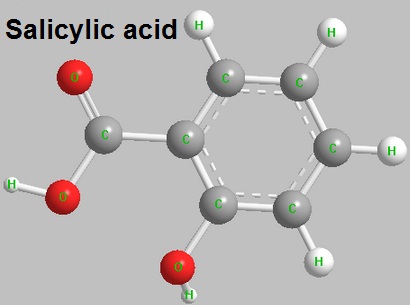
Figura1 La struttura dell’acido salicilico
L’acido salicilico ha capacità di sterilizzazione, la soluzione alcolica al 2,5% (chiamata spiritus) è usata come medicina topica nel trattamento della tinea manus e tinea pedis, inoltre può essere fatta in pomata. Il salicilato di sodio può essere usato per il conservante alimentare o i conservanti, inoltre può essere usato per la preparazione di dentifricio, collutorio. L’acido salicilico ha effetti antipiretici e analgesici, può curare i reumatismi e così via. Tutti i suoi esteri possono essere usati come droga e spezie. Il salicilato di metile ha piacevoli aromi di agrifoglio, è usato per la preparazione di profumo e sapore di sapone. Il salicilato di metile è rivestito sulla pelle, può penetrare nel muscolo e far uscire l’acido salicilico per rilasciare il dolore locale, quindi può anche essere usato per il trattamento del dolore, contusione, distorsione e altri farmaci. Isoamyl salicylate ha aroma di orchidea, benzyl salicylate ha debole aroma di estere, entrambi possono preparare profumo o sapore di sapone. Il nome comune del salicilato fenilico è Salo, è stato idrolizzato in fenolo e acido salicilico nell’intestino, è un tipo di efficaci conservanti enterali. Un altro farmaco gentile legato all’acido salicilico è l’acido para aminosalicilico (PAS, vedi “Para amino acido salicilico), i suoi sali di sodio e di calcio sono usati come farmaci anti TB per la tubercolosi polmonare acuta essudativa (TB) e la tubercolosi mucosa, è un farmaco antimicrobico debole, l’effetto è solo il 2% della streptomicina, spesso combinato con streptomicina e isoniazide, per migliorare l’effetto curativo. Può essere acetilato all’aspirina.
Le informazioni di cui sopra sono Chemicalbook Hanya modificato.
proprietà chimica
cristallo dell’ago 1.white o bordo monoclino cristallino, piccante. Leggermente solubile in acqua, solubile in acetone, olio di trementina, etanolo, etere etilico, benzene e cloroformio.2.L’acidità dell’acido salicilico è più forte dell’acido benzoico, diventa più scuro nel colore al sole. Nel caso dello ione ferro, diventa in chelato viola. Reagisce con cloruro ferrico per mostrare viola, è instabile al calore, facile alla decarbossilazione per produrre fenolo riscaldamento a 200 ℃. In natura l’acido salicilico è per lo più in forma di metile esistente nell’olio di corteccia di betulla, il contenuto è fino al 96%. Ci sono esistenti in olio di cannella, olio viola, olio wintergreen. L’acido salicilico libero solo pochi esistono nelle piante. L’acido salicilico ha una doppia proprietà di fenolo e acido carbossilico. Quando viene riscaldato, è sublimazione, e rapido riscaldato, si decompone in fenolo e anidride carbonica. Quando reagisce con idrossido di sodio, idrossile e gruppi carbossilici sono stati neutralizzati per produrre il sale doppio; ma con carbonato di sodio, solo i gruppi carbossilici sono neutralizzati e costruire un singolo sale. Quando reagisce con alcool o fenolo, può generare il corrispondente estere dell’acido carbossilico. Questo prodotto è tossico e irritante per la pelle, le mucose, e la reazione con la proteina del tessuto del corpo, quindi è corrosivo, da un altro aspetto, può essere sterilizzato. Ratti LD501100~1600mg/kg. La conservazione è stabile, ma la polvere e l’aria mescolate per produrre l’esplosione. Nell’industria, l’acido salicilico è stato preparato da fenolato di sodio e anidride carbonica nel sistema di reazione a pressione di riscaldamento (reazione di Kolbe Schmitt), il primo generato a sale di sodio di fenolo da idrossido di sodio neutralizzato con fenolo, e in 4 ~ 7 x 105 Pa (4 ~ 7 ATM) e 125 ℃, quindi assorbire anidride carbonica per generare benzene acido solfonico estere, da riorganizzazione per generare salicilato di sodio, e acidificazione per acido salicilico.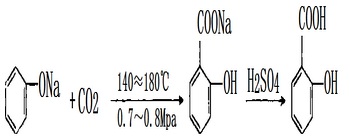
Proprietà fisiche
È polvere cristallina bianca, inodore, prima gusto amaro poi dolce. Esiste in natura nella corteccia di salice, nelle foglie e nella betulla dolce. La formula chimica di C6H4 (OH) (COOH), il punto di fusione è 157-159 ℃. Alla luce, si scolorisce gradualmente. La densità relativa è 1,44. Il punto di ebollizione è circa 211℃/2.67kPa. Sublimazione a 76℃. Sotto la pressione comune, rapido decomposto termico a fenolo e anidride carbonica. Solubile in etanolo, etere etilico, cloroformio, benzene, acetone, olio di trementina, insolubile in acqua. 1 g di acido salicilico è stato sciolto in 460 ml di acqua, 15 ml di acqua bollente, 2,7 ml di etanolo, 3 ml di acetone, 3 ml di etere, 42 ml di cloroformio, 135 ml di benzene, 52 ml di glicerolo di trementina, circa 60 ml di glicerolo e 80 ml di etere di petrolio. L’aggiunta di fosfato di sodio, borace può aumentare la solubilità dell’acido salicilico in acqua. Il PH della soluzione acquosa di acido salicilico è 2.4. L’acido alicilico reagisce con una soluzione acquosa di cloruro ferrico per generare una porpora speciale.
Ingredienti attivi per i farmaci contro l’acne
L’acido salicilico è un beta-idrossiacido che inoltre scortica l’accumulo di cellule morte all’interno del follicolo, agisce come un leggero antibatterico e ha proprietà lenitive. L’acido salicilico è considerato meno irritante del perossido di benzoile e ha meno potenziale di allergia, ma è anche meno aggressivo nel trattamento dell’acne. È spesso usato per trattare forme più lievi di acne. La concentrazione nei farmaci OTC è limitata al 2%. L’acido salicilico è anche usato come ingrediente esfoliante in concentrazioni più piccole, senza fare una dichiarazione di farmaco.
azione farmacologica
L’acido salicilico è ampiamente usato, eczema, psoriasi, acido salicilico può essere usato in acne, forfora. La concentrazione di 3%~6% può essere usata per cornea, superiore a 6% di acido salicilico può danneggiare il tessuto. Sotto il 40% di concentrazione è adatto per il trattamento di bozzolo spesso, calli e verruche. L’acido salicilico può anche essere aggiunto nel trattamento dell’acne e della forfora. Al giorno d’oggi molti ingredienti cosmetici famosi: nel 1993, Clinique CLINIQUE prima lanciato 1% di acido salicilico in crema di acqua dolce, divenne immediatamente uno dei prodotti di maggior successo di Clinique; Nel 1998, SK-II cristallo indotto crema pelle aggiunto 1,5%BHA ingredienti per l’originale, e l’acido salicilico ha effetto di trattamento pori e cutina come l’analogia uovo peeling che ha causato il boom del mercato; accesso aperto Olay popolare prodotti attivando crema contiene anche 1,5% BHA componenti. Tuttavia, a causa dell’alta concentrazione di acido salicilico, ha un certo grado di danno, cosmetici contenenti concentrazione di acido salicilico è stato generalmente limitato tra 0,2% ~ 1,5%, contenenti cosmetici acido salicilico deve essere aggiunto alla nota di segnali di avvertimento per determinare la sicurezza di uso a lungo termine e bambini sotto i 3 anni di età anche non deve essere utilizzato.
Contrasto con l’effetto di bellezza dell’acido
L’acido salicilico (BHA) è estratto dalla corteccia di salice, foglia di agrifoglio, chiamato anche acido vegetale; L’acido tartarico (AHA) è stato estratto dalla canna da zucchero; due diverse materie prime estrarre acido. I due possono controllare l’olio, cutina, rimuovere l’acne, restringere i pori, luce stampa. Più del 50% di concentrazione della pelle di cambiamento acido può essere operato solo dal medico di Dipartimento di Dermatologia, e non importa quanta concentrazione di acido salicilico, pelli sono classificati come trattamento medico, vale la pena notare che alcune persone non sono adatti per l’uso di qualsiasi concentrazione di acido salicilico, così il salone di bellezza generale non viene eseguito, sotto il 40% di acido salicilico nel salone di bellezza della pelle acido è consentito in legge, al contrario, l’acido tartarico è più sicuro di acido salicilico. Per quanto riguarda l’effetto dell’acido salicilico, l’acido salicilico solo bloccato nello strato corneo superficiale, solo giocare un semplice trattamento ed effetto di blocco, cambiando la pelle è solo temporaneo, mentre l’acido tartarico nella corteccia vero cambiato fondamentalmente. La pelle può essere curata, i pozzi di formazione del danno dermico, l’acido salicilico diventa incapace di azione, quindi non può essere chiamato pelle di acido salicilico, può essere chiamato solo trattamento di acido salicilico. La sicurezza dell’acido salicilico e dell’acido tartarico e l’effetto della pelle sono diversi, perché l’acido tartarico non è tossico, uso da basso ad alto (8%-15%-20%-30%-40%), lentamente adattamento non è bruciare la pelle, sfigurato e qualsiasi effetti collaterali. Mentre l’acido salicilico è tossico, alta concentrazione non è adatto per l’uso in faccia, ci sono alcune restrizioni sulla concentrazione, la concentrazione può essere utilizzato per la pelle nel 3%-6%, superiore al 6% acido salicilico è corrosivo per la pelle, un’alta concentrazione del 40% acido salicilico ha forti proprietà di corrosione della cheratina.
Usi
l’acido 1.Salicylic cioè l’acido ortho hydroxy benzoic (acido o-idrossibenzoico) è un genere di materia prima sintetica organica importante. Nella produzione di pesticidi, è usato per il fosforo organico sintetico pesticida Isocarbophos, isofenphos metile intermedi isopropilico salicilato e Rodenticide warfarin, uccidere ratti etere intermedio 4-idrossi cumarina; nell’industria farmaceutica, l’acido salicilico è stato usato come antisettici, anche come intermedi di acido acetilsalicilico (aspirina) e altri farmaci; è anche una materia prima importante di tintura, spezie, come l’industria della gomma.
2.It è utilizzato principalmente come materie prime di aspirina feedstock e pesticidi ammina acquosa e prodotti di fosforo, può anche essere utilizzato nell’industria tintoria, raffinazione e reagente chimico, ecc.
3.Used nell’industria farmaceutica per i farmaci antipiretici, analgesici, anti-infiammatori, diuretici, tintura industriale utilizzato per diretto di coloranti azoici e coloranti mordente acido, ma anche per le spezie, ecc
4.Used come indicatore complessante e conservante.
5.Verification per alluminio, boro, cerio, rame, ferro, piombo, manganese, mercurio, nichel, argento, titanio, tungsteno, vanadio, solfito, nitrato e nitrito. Determinazione di alluminio, rame, ferro, torio, titanio e uranio. Metodo alcalino e standard di titolazione iodometrica. L’indicatore fluorescente. Indicatore complessometrico.
6.L’acido salicilico è un’importante materia prima di medicina, spezie, coloranti, ausiliari della gomma e altri prodotti chimici fini. Nell’industria farmaceutica, l’acido salicilico stesso è usato come antisettico, per l’iperplasia cutanea locale e l’infezione fungina della pelle. Per quanto riguarda gli intermedi farmaceutici, è usato per la produzione di etenzamide, diuretina, acido acetilsalicilico (aspirina), salicilato di sodio e salicilamide, glibenclamide niclosamide, acido salicilico, estere fenilico, etile p-idrossibenzoato, subsalicilato di bismuto, sulfasalazina e altri farmaci. Nell’industria dei coloranti, è usato per la produzione del colorante diretto giallo GR, diretto grigio BL, diretto marrone chiaro RT, marrone mordente acido G, giallo mordente acido GG. Gli esteri dell’acido salicilico sono usati come spezia, per esempio, il salicilato di metile può essere usato come dentifricio e altre spezie orali e altre spezie e spezie alimentari. Usato nella produzione dell’industria della gomma agente antiscorching, assorbente ultravioletto e agente schiumogeno e acqua. L’acido salicilico può anche essere usato come agente di polimerizzazione delle resine fenoliche, stampa tessile e conservanti di polpa di tintura, tintura delle fibre sintetiche dell’agente di espansione (agente) e così via.
Metodi di produzione
1. Il fenolo e l’idrossido di sodio reagiscono per produrre il sodio del fenolo, la distillazione e la disidratazione, la reazione di carbossilazione di CO2 per ottenere il salicilato di sodio, quindi usando l’acido solforico e produrre il prodotto grezzo. Il prodotto grezzo attraverso la sublimazione raffinato al prodotto finito. Quota di consumo delle materie prime: fenolo (98%) 704kg/t, alcali bruciare (95%) 417kg/t, solfato (95%) 500kg/t, anidride carbonica (99%) 467kg/t.
2.Il metodo di preparazione del metodo è che il sale di sodio del fenolo e dell’anidride carbonica può essere ottenuto da acidification.
phenol e la soda caustica liquida sono prodotti nella soluzione del sale di sodio del fenolo, essiccazione di vuoto e poi a 100℃, lentamente messo all’anidride carbonica asciutta, quando la pressione raggiunge 0.7~0.8MPa, fermata che passa l’anidride carbonica, riscaldante fino a 140 a 180℃. Dopo la reazione con acqua, salicilato di sodio sciolto e decolorazione, filtraggio, accoppiato con l’acido solforico, cioè precipitazione acido salicilico, dopo il filtraggio, lavaggio e asciugatura per ottenere il prodotto.
Descrizione
L’acido salicilico (dal latino salix, salice, dalla cui corteccia si ottiene la sostanza) è un acido monoidrossi benzoico, un tipo di acido fenolico e un acido beta idrossilico. Questo acido organico cristallino incolore è ampiamente utilizzato nella sintesi organica e funziona come un ormone vegetale. Deriva dal metabolismo della salicina. Oltre ad essere un importante metabolita attivo dell’aspirina (acido acetilsalicilico), che agisce in parte come un prod rug all’acido salicilico, è probabilmente più conosciuto per il suo uso nei trattamenti anti-acne. I sali e gli esteri dell’acido salicilico sono conosciuti come salicilati.
Proprietà chimiche
L’acido salicilico ha la formula C6H4(OH) COOH, dove il gruppo OH è orto al gruppo carbossilico. È anche conosciuto come acido 2-idrossibenzoico. È scarsamente solubile in acqua (2 g/l a 20 °C). L’aspirina (acido acetilsalicilico o ASA) può essere preparata dall’esterificazione del gruppo idrossilico fenolico dell’acido salicilico con il gruppo acetile dell’anidride acetica o del cloruro di acetile.
Proprietà chimiche
L’acido 2-idrossibenzoico è inodore o ha un leggero odore fenolico con un sapore acre.
Proprietà chimiche
Conosciuto anche come acido o-idrossibenzoico, C6H4(OH)(COOH) è una polvere bianca con un gusto acre che è stabile in aria ma gradualmente scolorita dalla luce. Solubile in acetone, olio di trementina, alcool, etere, benzene; leggermente solubile in acqua e combustibile. Derivato dalla reazione di una soluzione calda di fenolato di sodio con anidride carbonica e dall’acidificazione del sale di sodio così formato. Usato nella fabbricazione di aspirina e salicilati, resine, colorante intermedio, inibitore di prevulcanizzazione, reagente analitico e fungicida.
Proprietà chimiche
L’acido salicilico è un cristallinesolido da bianco a marrone; aghi.
Eccursione
Frutta e verdure acerbe sono fonti naturali di acido salicilico, in particolare more, mirtilli, meloni, datteri, uva passa, kiwi, guaiave, albicocche, pepe verde, olive, pomodori, ravanelli e cicoria; anche funghi. Alcune erbe e spezie contengono quantità piuttosto elevate, anche se carne, pollame, pesce, uova e latticini hanno tutti poco o niente salicilati. Dei legumi, semi, noci e cereali, solo le mandorle, le castagne d’acqua e le arachidi hanno quantità significative.
Storia
Il medico greco Ippocrate scrisse nel V secolo a.C. di una polvere amara estratta dalla corteccia di salice che poteva alleviare i dolori e ridurre la febbre. Questo rimedio era anche menzionato in testi dell’antica Sumer, del Libano e dell’Asiria.
L’estratto attivo della corteccia, chiamato salicina, dal nome latino del salice bianco (Salix alba), fu isolato e nominato dal chimico tedesco Johann Andreas Buchner nel 1826. Raffaele Piria, un chimico italiano fu in grado di convertire la sostanza in uno zucchero e in un secondo componente, che all’ossidazione diventa acido salicilico.
L’acido salicilico fu anche isolato dall’erba olmaria (Filipendula ulmaria, precedentemente classificata come Spiraea ulmaria) da ricercatori tedeschi nel 1839. Mentre il loro estratto era in qualche modo efficace, ha anche causato problemi digestivi come irritazione gastrica, sanguinamento, diarrea e persino la morte se consumato in dosi elevate.
Usi
L’acido salicilico è noto per la sua capacità di alleviare i dolori e ridurre la febbre. Queste proprietà medicinali, in particolare la riduzione della febbre, sono note fin dall’antichità, ed è usato come farmaco antinfiammatorio.
Nella medicina moderna, l’acido salicilico e i suoi derivati sono usati come costituenti di alcuni prodotti rubefacenti. Per esempio, il salicilato di metile è usato come linimento per lenire i dolori articolari e muscolari, e il salicilato di colina è usato topicamente per alleviare il dolore delle afte. Come altri beta-idrossiacidi, l’acido salicilico è un ingrediente chiave in molti prodotti per la cura della pelle per il trattamento della dermatite seborroica, acne, psoriasi, calli, duroni, cheratosi pilaris e verruche.
Usi
Anche se tossico in grandi quantità, l’acido salicilico è usato come conservante alimentare e come battericida e antisettico. Per alcune persone con sensibilità al salicilato anche queste piccole dosi possono essere dannose.
Il salicilato di sodio è un fosforo utile nell’ultravioletto vuoto con efficienza quantica quasi piatta per lunghezze d’onda tra 10 e 100 nm. Fosfora nel blu a 420 nm. Si prepara facilmente su una superficie pulita spruzzando una soluzione satura del sale in metanolo seguita da evaporazione.
Usi
L’acido salicilico è un beta-idrossiacido con attività cheratolitica e antinfiammatoria. Aiuta a dissolvere lo strato superiore delle cellule dello strato corneo, migliorando l’aspetto e la sensazione della pelle. L’acido salicilico è un ingrediente efficace nei prodotti per l’acne e come tale è ampiamente utilizzato nei saponi e nelle lozioni per l’acne. Poiché è solubile nei lipidi, può ridurre più facilmente il blocco dei follicoli sebacei penetrando nei pori ed esfoliando l’accumulo cellulare. È antimicrobico, antisettico, migliora l’attività dei conservanti e può essere usato per regolare il pH dei prodotti. Per il trattamento della pelle che invecchia, sembra aiutare a migliorare le rughe, la rugosità e il tono della pelle. Inoltre, è un ingrediente utile per i prodotti formulati per trattare psoriasi, calli, calli e verruche – casi in cui c’è un accumulo di cellule morte della pelle. Quando viene applicato topicamente, è riportato che penetra da 3 a 4 mm nell’epidermide. Una piccola quantità di acido salicilico può convertirsi in salicilato di rame, un potente antinfiammatorio. usato ad alte concentrazioni, l’acido salicilico può causare arrossamenti ed eruzioni cutanee. Si tratta di un acido organico presente in natura, legato all’aspirina. Si trova in alcune piante, in particolare le foglie di wintergreen, la corteccia di salice e la corteccia di betulla dolce. L’acido salicilico è anche prodotto sinteticamente.
Usi
L’acido salicilico è un’impurità dell’acido acetilsalicilico (A187780). Impurità B dell’acido acetilsalicilico.
Usi
farmaci antinfiammatori non steroidei
Definizione
ChEBI: Un acido monoidrossibenzoico che è acido benzoico con un gruppo idrossi in posizione orto. Si ottiene dalla corteccia del salice bianco e dalle foglie del wintergreen.
Definizione
Un acido carbossilico cristallinoaromatico. È usato nelle medicine, come antisettico e nella fabbricazione di coloranti azoici. Il suo estere etanoilico (acetilico) è l’aspirina. Vedere aspirina; salicilato di metile.
Metodi di produzione
L’acido salicilico può essere ottenuto (1) dall’olio di wintergreen, che contiene salicilato di metile, o (2) riscaldando fenato di sodio secco C6H5ONa più anidride carbonica sotto pressione a 130 °C (266 °F) e recuperando dal salicilato di sodio risultante aggiungendo acido solforico diluito.
Indicazioni
L’acido salicilico è un β-idrossiacido che penetra nella ghiandola sebacea e ha proprietà comedolitiche e antinfiammatorie. Può essere usato come terapia aggiuntiva e si trova in detergenti, tonici, maschere e peel.
L’acido salicilico è cheratolitico e a concentrazioni tra il 3% e il 6% provoca l’ammorbidimento degli strati cornei e lo spargimento delle squame. Produce questa desquamazione solubilizzando il cemento intercellulare e migliora lo spargimento dei corneociti diminuendo la coesione tra le cellule. In concentrazioni > del 6%, può essere distruttivo per il tessuto. L’applicazione di grandi quantità della più alta concentrazione di acido salicilico può anche provocare una tossicità sistemica. L’acido salicilico è usato nel trattamento delle infezioni superficiali-fungine, acne, psoriasi, dermatite seborroica, verruche e altre dermatosi desquamanti. Quando è combinato con zolfo, alcuni credono che un effetto sinergico cheratolitico è prodotto. Le preparazioni comuni includono un unguento al 3% e al 6% con uguale concentrazione di zolfo; una soluzione al 6% di glicole propilenico (Keralyt); dal 5% al 20% con parti uguali di acido lattico in collodio flessibile per le verruche (Duofilm, Occlusal); in una base di crema a qualsiasi concentrazione per effetti cheratolitici; come unguento al 60% per le verruche plantari; e in un cerotto al 40% su tessuto di velluto per il trattamento di calli e verruche (cerotto al 40% di acido salicilico).
Preparazione
Preparato riscaldando il fenolato di sodio con anidride carbonica sotto pressione
Metodi di produzione
L’acido salicilico è biosintetizzato dall’aminoacido fenilalanina. Nell’Arabidopsis thaliana può anche essere sintetizzato attraverso una via indipendente dalla fenilalanina.
Il salicilato di sodio è preparato commercialmente trattando il fenolato di sodio (il sale di sodio del fenolo) con anidride carbonica ad alta pressione (100 atm) e alta temperatura (390K) – un metodo noto come reazione di Kolbe-Schmitt. L’acidificazione del prodotto con acido solforico dà acido salicilico :
Può anche essere preparato dall’idrolisi dell’aspirina (acido acetilsalicilico) o del salicilato di metile (olio di verde inverno) con un acido o una base forte.
nome della marca
Advanced Pain Relief Callus Removers (Schering-Plough HealthCare); Advanced Pain Relief Corn Removers (Schering-Plough HealthCare); Clear Away Wart Remover (Schering-Plough HealthCare); Compound W (Whitehall-Robins); Dr. Scholl’s Callus Removers (Schering-Plough HealthCare); Dr. Scholl’s Corn Removers (Schering-Plough HealthCare); Dr. Scholl’s Wart Remover Kit (Schering-Plough HealthCare); Duofilm Wart Remover (Schering-Plough HealthCare); Duoplant (Stiefel); Freezone (Whitehall-Robins); Ionil (Galderma); Ionil-Plus (Galderma); Salicylic Acid Soap (Stiefel); Saligel (Stiefel); Stri-Dex (Sterling Health U.S.A.).
Riferimento(i) di sintesi
The Journal of Organic Chemistry, 27, p. 3551, 1962 DOI: 10.1021/jo01057a035
Tetrahedron Letters, 37, p. 153, 1996 DOI: 10.1016/0040-4039(95)02120-5
Descrizione generale
Bianco inodore a solido marrone chiaro. Affonda e si mescola lentamente con l’acqua.
Aria & Reazioni con l’acqua
Sublima e forma vapore o polvere che può esplodere.
Profilo di reattività
L’acido salicilico è un acido carbossilico. Gli acidi carbossilici donano ioni idrogeno se è presente una base che li accetta. Reagiscono in questo modo con tutte le basi, sia organiche (per esempio, le ammine) che inorganiche. Le loro reazioni con le basi, chiamate “neutralizzazioni”, sono accompagnate dall’evoluzione di notevoli quantità di calore. La neutralizzazione tra un acido e una base produce acqua più un sale. Gli acidi carbossilici con sei o meno atomi di carbonio sono liberamente o moderatamente solubili in acqua; quelli con più di sei carboni sono leggermente solubili in acqua. Gli acidi carbossilici solubili si dissociano in una certa misura in acqua per produrre ioni idrogeno. Il pH delle soluzioni di acidi carbossilici è quindi inferiore a 7,0. Molti acidi carbossilici insolubili reagiscono rapidamente con soluzioni acquose contenenti una base chimica e si dissolvono perché la neutralizzazione genera un sale solubile. Gli acidi carbossilici in soluzione acquosa e gli acidi carbossilici liquidi o fusi possono reagire con i metalli attivi per formare idrogeno gassoso e un sale metallico. Tali reazioni si verificano in linea di principio anche per gli acidi carbossilici solidi, ma sono lente se l’acido solido rimane asciutto. Anche gli acidi carbossilici “insolubili” possono assorbire abbastanza acqua dall’aria e dissolversi sufficientemente in acido salicilico per corrodere o dissolvere parti e contenitori di ferro, acciaio e alluminio. Gli acidi carbossilici, come altri acidi, reagiscono con i sali di cianuro per generare idrogeno cianuro gassoso. La reazione è più lenta per gli acidi carbossilici secchi e solidi. Gli acidi carbossilici insolubili reagiscono con soluzioni di cianuri per causare il rilascio di acido cianidrico gassoso. Gas infiammabili e/o tossici e calore sono generati dalla reazione degli acidi carbossilici con composti diazo, ditiocarbammati, isocianati, mercaptani, nitruri e solfuri. Gli acidi carbossilici, specialmente in soluzione acquosa, reagiscono anche con solfiti, nitriti, tiosolfati (per dare H2S e SO3), ditioniti (SO2), per generare gas infiammabili e/o tossici e calore. La loro reazione con carbonati e bicarbonati genera un gas innocuo (anidride carbonica) ma ancora calore. Come altri composti organici, gli acidi carbossilici possono essere ossidati da forti agenti ossidanti e ridotti da forti agenti riducenti. Queste reazioni generano calore. È possibile una grande varietà di prodotti. Come altri acidi, gli acidi carbossilici possono iniziare reazioni di polimerizzazione; come altri acidi, spesso catalizzano (aumentano il tasso di) reazioni chimiche.
Pericolo
Alcalosi respiratoria, iperkaliemia, ipertermia, disidratazione, convulsioni, shock, paralisi res-piratoria, acidosi respiratoria, lesioni e morte per collasso respiratorio; fetotossico.
Pericolo per la salute
L’inalazione della polvere irrita il naso e la gola. Il vomito può verificarsi spontaneamente se grandi quantità vengono ingerite. Il contatto con gli occhi causa irritazione, dolore marcato e lesioni corneali che dovrebbero guarire. Il contatto prolungato o ripetuto con la pelle può causare un’irritazione marcata o anche una leggera ustione.
Meccanismo d’azione
L’acido salicilico ha dimostrato di funzionare attraverso diversi percorsi. Produce i suoi effetti anti – infiammatori sopprimendo l’attività della ciclossigenasi (COX), un enzima responsabile della produzione di mediatori pro – infiammatori come le prostaglandine. In particolare, non lo fa attraverso l’inibizione diretta della COX, a differenza della maggior parte degli altri farmaci antinfiammatori non steroidei (FANS), ma invece attraverso la soppressione dell’espressione dell’enzima (attraverso un meccanismo non ancora chiarito). L’acido salicilico ha anche dimostrato di attivare l’adenosina monofosfato-attivata protein chinasi (AMPK), e si pensa che questa azione possa giocare un ruolo negli effetti antitumorali del composto e dei suoi prodotti aspirina e salsalato. Inoltre, gli effetti anti diabetici dell’acido salicilico sono probabilmente mediati dall’attivazione di AMPK principalmente attraverso un cambiamento conformazionale allosterico che aumenta i livelli di fosforilazione. L’acido salicilico disaccoppia anche la fosforilazione ossidativa che porta ad un aumento dei rapporti ADP:ATP e AMP:ATP nella cellula. Di conseguenza, l’acido salicilico può alterare l’attività dell’AMPK e successivamente esercitare le sue proprietà antidiabetiche attraverso un alterato stato energetico della cellula. Anche nei topi knock-out AMPK, tuttavia, c’è un effetto antidiabetico che dimostra che c’è almeno un’ulteriore azione non ancora identificata del composto.
Effetti collaterali
Gli effetti collaterali dell’acido salicilico includono eritema e desquamazione.
Profilo di sicurezza
Veleno per ingestione, via endovenosa e intraperitoneale. Moderatamente tossico per via sottocutanea. Un teratogeno sperimentale. Effetti sistemici umani per contatto con la pelle: tinnito auricolare. Dati di mutazione riportati. Irritante per la pelle e per gli occhi. Effetti riproduttivi sperimentali. Incompatibile con sali di ferro, etere nitroso, acetato di piombo, iodio. Usato nella produzione di aspirina. Se riscaldato fino alla decomposizione emette fumo acre e fumi irritanti.
Esposizione potenziale
Usato come agente cheratolitico topico; nella produzione di aspirina, salicilati, resine, come colorante intermedio; inibitore di prevulcanizzazione; reagente analitico; fungicida, antisettico e conservante alimentare.
Droghe e trattamenti veterinari
Spesso combinati con lo zolfo, gli shampoo all’acido salicilico sono spesso impiegati per trattare i pazienti con disturbi seborroici (seborrea sicca andoleosa) che presentano una desquamazione da lieve a moderata, con lievi detriti cerosi e cheratinici. In concentrazioni più elevate, topici come Kerasolv?Gel (6,6% di acido salicilico) possono essere utilizzati per rimuovere i tessuti eccessivi localizzati associati a disturbi ipercheratotici, come calli e ispessimenti idiopatici del planum nasale e delle piante dei piedi.
L’acido salicilico ha azioni leggermente antipruritiche, antibatteriche (batteriostatiche), cheratoplastiche e cheratolitiche. Le concentrazioni più basse sono principalmente cheratoplastiche e quelle più alte cheratolitiche. L’acido salicilico abbassa il pH della pelle, aumenta l’idratazione dei corneociti e dissolve il legante intercellulare tra i corneociti. Si pensa che l’acido salicilico e lo zolfo siano sinergici nelle loro azioni cheratolitiche.
Metodi di purificazione
È stato purificato per distillazione a vapore, per ricristallizzazione da H2O (la solubilità è 0,22% a temperatura ambiente e 6,7% a 100o), MeOH assoluto, o cicloesano e per sublimazione sotto vuoto a 76o. Il cloruro acido (aghi) ha m 19-19.5o, b 92o/15mm, l’ammide ha m 133o (aghi gialli da H2O), il derivato O-acetilico ha m 135o (riscaldamento rapido e il liquido resolidifica a 118o), e il derivato O-benzoilico ha m 132o (EtOH acquoso). .
Ormone vegetale
L’acido salicilico (SA) è un fito-ormone fenolico e si trova nelle piante con ruoli nella crescita e nello sviluppo delle piante, nella fotosintesi, nella traspirazione, nell’assorbimento e nel trasporto di ioni. SA induce anche cambiamenti specifici nell’anatomia delle foglie e nella struttura dei cloroplasti. SA è coinvolta nella segnalazione endogena, mediando nella difesa delle piante contro i patogeni. Gioca un ruolo nella resistenza ai patogeni inducendo la produzione di proteine legate alla patogenesi. È coinvolto nella resistenza sistemica acquisita (SAR) in cui un attacco patogeno su una parte della pianta induce resistenza in altre parti. Il segnale può anche trasferirsi alle piante vicine tramite la conversione dell’acido salicilico nell’estere volatile, il salicilato di metile.
Incompatibilità
sali di ferro; acetato di piombo; iodio. Forma una miscela esplosiva in aria.