Propiedades químicas del ácido salicílico, usos, producción
Importantes materiales sintéticos orgánicos
El ácido salicílico es una importante materia prima sintética orgánica, ampliamente utilizada en medicina, pesticidas, tintes, caucho, alimentos y perfumes. En la industria farmacéutica, las principales producciones de ácido salicílico son el salicilato de sodio, el aceite de gaulteria (salicilato de metilo), la aspirina (ácido acetilsalicílico), la amina de ácido salicílico, el salicilato de fenilo. En la industria de los tintes, se utiliza para la producción de mordiente amarillo puro, amarillo directo 3GN, amarillo directo GR, marrón directo 3GN, mordiente ácido marrón G, mordiente ácido amarillo GG, complejo de tinte amarillo ácido. En la producción de plaguicidas, el ácido salicílico se utiliza para la síntesis del plaguicida orgánico de fósforo Isocarbophos, el intermedio salicilato de isopropilo isofenfos metilo y el rodenticida warfarina, el intermedio coumatetralilo 4-hidroxicumarina. En la industria del caucho, se utiliza como agente anti-quemadura y la producción de absorbente ultravioleta y agente espumante. Es material de perfume, utilizado para la preparación de salicilato de metilo, éster etílico del ácido salicílico; conservantes de alimentos, su sal de sodio se utiliza sobre todo, ahora un número de países han sido prohibidos; salicilato de metilo se puede utilizar como agentes de limpieza oral, como el sabor de la pasta de dientes.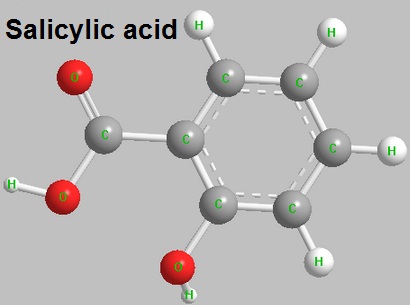
Figura1 La estructura del ácido salicílico
El ácido salicílico tiene capacidad de esterilización, la solución de alcohol al 2,5% (llamada spiritus) se utiliza como medicina tópica en el tratamiento de la tinea manus y la tinea pedis, también se puede convertir en pomada. El salicilato de sodio se puede utilizar como conservante de alimentos o conservantes, también se puede utilizar para la preparación de pasta de dientes, enjuague bucal. El ácido salicílico tiene efectos antipiréticos y analgésicos, puede curar el reumatismo, etc. Todos sus ésteres pueden ser utilizados como droga y especias. El salicilato de metilo tiene agradables aromas de acebo, se utiliza para la preparación de perfumes y sabor de jabón. El salicilato de metilo se recubre en la piel, puede penetrar en el músculo y dejar salir el ácido salicílico para liberar el dolor local, por lo que también se puede utilizar para el tratamiento del dolor, contusión, esguince y otros medicamentos. El salicilato de isoamilo tiene aroma de orquídea, el salicilato de bencilo tiene aroma de éster débil, ambos pueden preparar el perfume o el sabor del jabón. El nombre común de salicilato de fenilo es Salo, se hidroliza en fenol y ácido salicílico en el intestino , es una especie de conservantes enterales eficaces. Otro fármaco amable relacionado con el ácido salicílico es el ácido para aminosalicílico (PAS, véase «ácido para amino salicílico»), Sus sales de sodio y calcio se utilizan como fármacos contra la tuberculosis pulmonar exudativa aguda (TB) y la tuberculosis de la mucosa, es un fármaco antimicrobiano débil, el efecto es sólo el 2% de la estreptomicina, a menudo combinado con estreptomicina e isoniazida , con el fin de mejorar el efecto curativo. Puede ser acetilado a la aspirina.
La información anterior es Chemicalbook Hanya editado.
propiedades químicas
1.Cristal de aguja blanco o borde monoclínico cristalino, picante. Ligeramente soluble en agua, soluble en acetona, aceite de trementina, etanol, éter etílico, benceno y cloroformo.2.La acidez del ácido salicílico es más fuerte que la del ácido benzoico, se oscurece al sol. En el caso del ion hierro, se convierte en quelato púrpura. Reacciona con el cloruro férrico para mostrar el color púrpura, es inestable al calor, fácil de descarboxilación para producir fenol calentando a 200 ℃. En la naturaleza, el ácido salicílico se encuentra principalmente en forma de metilo, y su contenido en el aceite de corteza de abedul alcanza el 96%. Existe en el aceite de canela, aceite de violeta, aceite de gaulteria. El ácido salicílico libre sólo existe en unas pocas plantas.ácido salicílico tiene la doble propiedad de fenol y ácido carboxílico. Cuando se calienta, se sublima, y cuando se calienta rápidamente, se descompone en fenol y dióxido de carbono. Cuando reacciona con hidróxido de sodio, los grupos hidroxilo y carboxilo se neutralizan para producir la sal doble; pero con el carbonato de sodio, sólo se neutralizan los grupos carboxilo y se construye una única sal. Cuando reacciona con alcohol o fenol, puede generar el correspondiente éster de ácido carboxílico. Este producto es tóxico e irritante para la piel, la membrana mucosa, y reacciona con la proteína del tejido corporal, por lo que es corrosivo, desde otro aspecto, puede ser esterilizado. Ratas LD501100~1600mg/kg. El almacenamiento es estable, pero el polvo y el aire se mezclan para producir una explosión. En la industria, el ácido salicílico fue preparado por fenolato de sodio y dióxido de carbono en el sistema de reacción de presión de calentamiento (reacción de Kolbe Schmitt), el primero generado a la sal de sodio de fenol por hidróxido de sodio neutralizado con fenol, y en 4 ~ 7 x 105 Pa (4 ~ 7 ATM) y 125 ℃, a continuación, absorber el dióxido de carbono para generar éster de ácido sulfónico de benceno, por reordenación para generar salicilato de sodio, y la acidificación al ácido salicílico.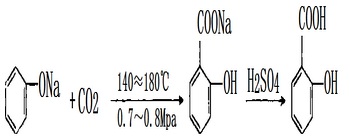
Propiedades físicas
Es un polvo cristalino blanco, inodoro, de sabor primero amargo y luego dulce. Existe en la naturaleza de la corteza del sauce, las hojas y el abedul dulce. La fórmula química de C6H4 (OH) (COOH), el punto de fusión es 157-159 ℃. En la luz, se decolora gradualmente. La densidad relativa es de 1,44. El punto de ebullición es de unos 211℃/2,67kPa. La sublimación es de 76℃. Bajo la presión común, se descompone térmicamente de forma rápida en fenol y dióxido de carbono. Soluble en etanol, éter etílico, cloroformo, benceno, acetona, aceite de trementina, insoluble en agua. Se disolvió 1g de ácido salicílico en 460ml de agua, 15ml de agua hirviendo, 2,7ml de etanol, 3ml de acetona, 3ml de éter, 42ml de cloroformo, 135ml de benceno, 52ml de trementina de glicerina, unos 60ml de glicerol y 80ml de éter de petróleo. La adición de fosfato de sodio, bórax puede aumentar la solubilidad del ácido salicílico en el agua. El PH de la solución acuosa de ácido salicílico es de 2,4. El ácido alicílico reacciona con la solución acuosa de cloruro férrico para generar un color púrpura especial.
Ingredientes activos de los medicamentos para el acné
El ácido salicílico es un beta-hidroxiácido que también desprende la acumulación de células muertas dentro del folículo, actúa como un antibacteriano suave y tiene propiedades calmantes. Se considera que el ácido salicílico es menos irritante que el peróxido de benzoilo y tiene menos potencial de alergia, pero también es menos agresivo en el tratamiento del acné. Suele utilizarse para tratar las formas más leves de acné. La concentración en los medicamentos de venta libre está limitada al 2%. El ácido salicílico también se utiliza como ingrediente de rendimiento exfoliante en concentraciones más pequeñas, sin hacer una declaración de drogas.
acción farmacológica
El ácido salicílico es ampliamente utilizado, eczema, psoriasis, el ácido salicílico puede ser utilizado en el acné, la caspa. La concentración de 3% ~ 6% se puede utilizar a la córnea, más de 6% de ácido salicílico puede dañar el tejido . Por debajo del 40% de concentración es adecuado para el tratamiento de capullo grueso, callos y verrugas. El ácido salicílico también se puede añadir en el tratamiento del acné y la caspa. Hoy en día muchos ingredientes cosméticos famosos: en 1993, Clinique CLINIQUE lanzó por primera vez el ácido salicílico al 1% en crema de agua blanda, inmediatamente se convirtió en uno de los productos más exitosos de Clinique; En 1998, la crema de piel inducida por el cristal de SK-II añadió 1,5%BHA ingredientes a la original, y el ácido salicílico tiene efecto de tratamiento de los poros y cutin como la analogía de pelar el huevo que causó el boom del mercado; acceso abierto Olay productos populares activando crema también contiene 1,5% BHA componentes. Sin embargo, debido a la alta concentración de ácido salicílico, tiene un cierto grado de daño, los cosméticos que contienen la concentración de ácido salicílico generalmente se ha limitado entre el 0,2% ~ 1,5%, que contiene cosméticos de ácido salicílico se añadirá a la nota de las señales de advertencia para determinar la seguridad del uso a largo plazo y los niños menores de 3 años de edad también no debe ser utilizado.
Contraste con el efecto de belleza del ácido
El ácido salicílico (BHA) se extrae de la corteza de sauce , hoja de acebo, también llamado ácido vegetal; el ácido tartárico (AHA) se extrajo de la caña de azúcar; dos materias primas diferentes extraen el ácido. Los dos pueden controlar el aceite, cutin, eliminar el acné, reducir los poros, la luz de impresión. Más del 50% de concentración de la piel de cambio de ácido puede ser operado por sólo el médico del Departamento de Dermatología, y no importa la concentración de ácido salicílico, las pieles se clasifican como tratamiento médico, vale la pena señalar que algunas personas no son adecuados para el uso de cualquier concentración de ácido salicílico, por lo que el salón de belleza en general no se ejecuta, por debajo del 40% de ácido salicílico en el salón de belleza de la piel de ácido se permite en la ley, en cambio, el ácido tartárico es más seguro que el ácido salicílico. En cuanto al efecto del ácido salicílico, el ácido salicílico sólo encerrado en el estrato córneo superficial, sólo jugar un simple tratamiento y el efecto de bloqueo, el cambio de la piel es sólo temporal, mientras que el ácido tartárico en la verdadera corteza cambiado fundamentalmente. La piel se puede curar, la formación de daños dérmicos pox pits, el ácido salicílico se vuelve incapaz de acción, por lo que no puede ser llamado ácido salicílico piel, sólo puede ser llamado tratamiento de ácido salicílico. La seguridad del ácido salicílico y el ácido tartárico y el efecto de la piel son diferentes, porque el ácido tartárico no es tóxico, el uso de baja a alta (8%-15%-20%-30%-40%), poco a poco la adaptación no es quemar la piel, desfigurado y cualquier efecto secundario. Mientras que el ácido salicílico es tóxico, de alta concentración no es adecuado para su uso en la cara, hay ciertas restricciones en la concentración, la concentración se puede utilizar a la piel en el 3%-6%, más de 6% de ácido salicílico es corrosivo para la piel, una alta concentración de ácido salicílico 40% tiene fuertes propiedades de corrosión de la queratina.
Usos
1.El ácido salicílico, es decir, el ácido ortohidroxibenzoico (ácido o-hidroxibenzoico) es un tipo de materia prima orgánica sintética importante. En la producción de plaguicidas, se utiliza para el plaguicida de fósforo orgánico sintético Isocarbophos, isofenphos intermedios de salicilato de isopropilo y Rodenticide warfarina, matar a las ratas éter intermedio 4-hidroxi cumarina; en la industria farmacéutica, el ácido salicílico se utilizó como antisépticos, también como intermedios de ácido acetilsalicílico (aspirina) y otras drogas; también es una importante materia prima de tinte, especias, como la industria del caucho.
2.Se utiliza principalmente como materia prima de la materia prima de la aspirina y pesticidas amina acuosa y productos de fósforo, también se puede utilizar en la industria de los tintes, el refinado y reactivo químico, etc.
3.Se utiliza en la industria farmacéutica para el antipirético, analgésico, antiinflamatorio, medicamentos diuréticos, tinte industrial utilizado para el directo de los tintes azoicos y tintes ácidos mordiente, sino también para las especias, etc.
4.Used como indicador complejante y preservative.
5.Verification para el aluminio, el boro, el cerio, el cobre, el hierro, el plomo, el manganeso, el mercurio, el níquel, la plata, el titanio, el tungsteno, el vanadio, el sulfito, el nitrato y el nitrito. Determinación de aluminio, cobre, hierro, torio, titanio y uranio. Método de los álcalis y estándar de valoración por iodometría. El indicador fluorescente. Indicador complexométrico.
6.El ácido salicílico es una importante materia prima de la medicina, las especias, los tintes, los auxiliares del caucho y otros productos químicos finos. En la industria farmacéutica, el ácido salicílico en sí mismo se utiliza como antiséptico, para la hiperplasia cutánea local y la infección por hongos en la piel. En cuanto a los productos farmacéuticos intermedios, se utiliza para la producción de etenzamida, diuretina, ácido acetilsalicílico (aspirina), salicilato de sodio y salicilamida, glibenclamida niclosamida, ácido salicílico, éster de fenilo, p-hidroxibenzoato de etilo, subsalicilato de bismuto, sulfasalazina y otros medicamentos. En la industria de los tintes, se utiliza para la producción de amarillo directo GR, gris directo BL, marrón claro directo RT, marrón mordiente ácido G, tinte amarillo mordiente ácido GG. Los ésteres del ácido salicílico se utilizan como especia, por ejemplo, el salicilato de metilo se puede utilizar como pasta de dientes y otras especias orales y otras especias y alimentos. Se utiliza en la producción de la industria del caucho como agente antiescorbante, absorbente ultravioleta y agente espumante y agua. El ácido salicílico también se puede utilizar como un agente de curado de resina fenólica, impresión textil y conservantes de la pulpa de teñido, teñido de fibra sintética del agente de expansión (agente) y así sucesivamente.
Métodos de producción
1. El fenol y el hidróxido de sodio reaccionan para producir fenol sódico, destilación y deshidratación, reacción de carboxilación de CO2 para obtener salicilato de sodio, luego usando ácido sulfúrico y producir el producto crudo. El producto crudo a través de la sublimación refinado al producto terminado. Cuota de consumo de materias primas: fenol (98%) 704kg/t, álcali quemado (95%) 417kg/t, sulfato (95%) 500kg/t, dióxido de carbono (99%) 467kg/t.
2.El método de preparación del método es que la sal de sodio de fenol y el dióxido de carbono se puede obtener por acidificación.
El fenol y la soda cáustica líquida se producen en la solución de la sal de sodio de fenol, el secado al vacío, y luego a 100℃, poner lentamente al dióxido de carbono seco, cuando la presión alcanza 0,7~0,8MPa, dejar de pasar el dióxido de carbono, el calentamiento de 140 a 180℃. Después de la reacción con agua, salicilato de sodio disuelto y decoloración, filtrado, acoplado con el ácido sulfúrico, a saber, la precipitación de ácido salicílico, después de filtrar, lavar y secar para obtener el producto.
Descripción
El ácido salicílico (del latín salix, sauce, de cuya corteza se obtiene la sustancia) es un ácido mono hidroxi benzoico, un tipo de ácido fenólico y un beta hidroxi ácido. Este ácido orgánico cristalino e incoloro se utiliza ampliamente en la síntesis orgánica y funciona como una hormona vegetal. Se deriva del metabolismo de la salicina. Además de ser un importante metabolito activo de la aspirina (ácido acetilsalicílico), que actúa en parte como un prodroga del ácido salicílico, es probablemente más conocido por su uso en tratamientos antiacné. Las sales y ésteres del ácido salicílico se conocen como salicilatos.
Propiedades químicas
El ácido salicílico tiene la fórmula C6H4(OH) COOH, donde el grupo OH está orto al grupo carboxilo. También se conoce como ácido 2-hidroxibenzoico. Es poco soluble en agua (2 g/l a 20 °C). La aspirina (ácido acetil salicílico o ASA) puede prepararse mediante la esterificación del grupo hidroxilo fenólico del ácido salicílico con el grupo acetilo del anhídrido acético o del cloruro de acetilo.
Propiedades químicas
El ácido 2-hidroxibenzoico es inodoro o tiene un ligero olor fenólico con un sabor acre.
Propiedades químicas
También conocido como ácido o-hidroxibenzoico, C6H4(OH)(COOH) es un polvo blanco con un sabor acre que es estable en el aire pero que se decolora gradualmente con la luz. Es soluble en acetona, aceite de trementina, alcohol, éter, benceno; ligeramente soluble en agua y combustible. Se obtiene haciendo reaccionar una solución caliente de fenolato de sodio con dióxido de carbono y acidificando la sal de sodio así formada. Se utiliza en la fabricación de aspirina y salicilatos, resinas, intermedio de colorantes, inhibidor de la prevulcanización, reactivo analítico y fungicida.
Propiedades químicas
El ácido salicílico es un sólido cristalino de color blanco a bronceado; agujas.
Ocurrencia
Las frutas y verduras inmaduras son fuentes naturales de ácido salicílico, especialmente las moras, los arándanos, los melones, los dátiles, las pasas, los kiwis, las guayabas, los albaricoques, los pimientos verdes, las aceitunas, los tomates, los rábanos y las achicorias; también las setas. Algunas hierbas y especias contienen cantidades bastante elevadas, aunque la carne, las aves de corral, el pescado, los huevos y los productos lácteos apenas contienen salicilatos. De las legumbres, semillas, frutos secos y cereales, sólo las almendras, las castañas de agua y los cacahuetes tienen cantidades significativas.
Historia
El médico griego Hipócrates escribió en el siglo V a.C. sobre un polvo amargo extraído de la corteza del sauce que podía aliviar los dolores y reducir la fiebre. Este remedio también se menciona en textos de la antigua Sumeria, Líbano y Asiria.
El extracto activo de la corteza, llamado salicina, por el nombre latino del sauce blanco (Salix alba), fue aislado y nombrado por el químico alemán Johann Andreas Buchner en 1826. Raffaele Piria, un químico italiano, fue capaz de convertir la sustancia en un azúcar y un segundo componente, que al oxidarse se convierte en ácido salicílico.
El ácido salicílico también fue aislado de la hierba reina de los prados (Filipendula ulmaria, antes clasificada como Spiraea ulmaria) por investigadores alemanes en 1839. Aunque su extracto era algo eficaz, también causaba problemas digestivos como irritación gástrica, hemorragias, diarrea e incluso la muerte cuando se consumía en dosis elevadas.
Usos
El ácido salicílico es conocido por su capacidad para aliviar los dolores y reducir la fiebre. Estas propiedades medicinales, en particular el alivio de la fiebre, se conocen desde la antigüedad, y se utiliza como medicamento antiinflamatorio.
En la medicina moderna, el ácido salicílico y sus derivados se utilizan como componentes de algunos productos rubefacientes. Por ejemplo, el salicilato de metilo se utiliza como linimento para calmar los dolores articulares y musculares, y el salicilato de colina se utiliza de forma tópica para aliviar el dolor de las úlceras bucales. Al igual que otros betahidroxiácidos, el ácido salicílico es un ingrediente clave en muchos productos para el cuidado de la piel para el tratamiento de la dermatitis seborreica, el acné, la psoriasis, las callosidades, los callos, la queratosis pilaris y las verrugas.
Usos
Aunque es tóxico en grandes cantidades, el ácido salicílico se utiliza como conservante de alimentos y como bactericida y antiséptico. Para algunas personas con sensibilidad al salicilato, incluso estas pequeñas dosis pueden ser perjudiciales.
El salicilato de sodio es un fósforo útil en el ultravioleta de vacío con una eficiencia cuántica casi plana para las longitudes de onda entre 10 y 100 nm . Es fluorescente en el azul a 420 nm. Se prepara fácilmente sobre una superficie limpia pulverizando una solución saturada de la sal en metanol seguida de evaporación.
Usos
El ácido salicílico es un beta-hidroxiácido con actividad queratolítica y antiinflamatoria. Ayuda a disolver la capa superior de células del estrato córneo, mejorando el aspecto y el tacto de la piel. El ácido salicílico es un ingrediente eficaz en los productos para el acné y, como tal, se utiliza ampliamente en jabones y lociones para el acné. Al ser soluble en lípidos, puede reducir más fácilmente la obstrucción del folículo sebáceo al penetrar en los poros y exfoliar la acumulación celular. Es antimicrobiano, antiséptico, potencia la actividad de los conservantes y puede utilizarse para ajustar el pH de los productos. Para el tratamiento de la piel envejecida, parece ayudar a mejorar las arrugas, la rugosidad y el tono de la piel. Además, es un ingrediente útil para los productos formulados para tratar la psoriasis, las callosidades, los callos y las verrugas, casos en los que hay una acumulación de células cutáneas muertas. Cuando se aplica de forma tópica, penetra de 3 a 4 mm en la epidermis. Una pequeña cantidad de ácido salicílico puede convertirse en salicilato de cobre, un potente antiinflamatorio. Utilizado en altas concentraciones, el ácido salicílico puede causar enrojecimiento de la piel y erupciones. Se trata de un ácido orgánico de origen natural, relacionado con la aspirina. Se encuentra en algunas plantas, especialmente en las hojas de gaulteria, la corteza del sauce y la corteza del abedul dulce. El ácido salicílico también se fabrica sintéticamente.
Usos
El ácido salicílico es una impureza del ácido acetilsalicílico (A187780). Ácido acetilsalicílico Impureza B.
Usos
antiinflamatorios no esteroideos
Definición
ChEBI: Es un ácido monohidroxibenzoico que es ácido benzoico con un grupo hidroxi en la posición orto. Se obtiene de la corteza del sauce blanco y de las hojas de gaulteria.
Definición
Es un ácido carboxílico cristalinoaromático. Se utiliza en medicamentos, como antiséptico y en la fabricación de colorantes azoicos. Su éster etanoil (acetil) es la aspirina. Véase aspirina; salicilato de metilo.
Métodos de producción
El ácido salicílico puede obtenerse (1) a partir del aceite de gaulteria, que contiene salicilato de metilo, o (2) calentando fenato de sodio seco C6H5ONa más dióxido de carbono bajo presión a 130 °C (266 °F) y recuperando del salicilato de sodio resultante añadiendo ácido sulfúrico diluido.
Instrucciones
El ácido salicílico es un β-hidroxiácido que penetra en la glándula sebácea y tiene propiedades comedolíticas y antiinflamatorias. Se puede utilizar como terapia coadyuvante y se encuentra en limpiadores, tónicos, mascarillas y peelings.
El ácido salicílico es queratolítico y en concentraciones entre el 3% y el 6% provoca el ablandamiento de las capas córneas y la caída de las escamas. Produce esta descamación mediante la solubilización del cemento intercelular y potencia el desprendimiento de los corneocitos mediante la disminución de la cohesión célula a célula. En concentraciones >6%, puede ser destructivo para los tejidos. La aplicación de grandes cantidades de la concentración más alta de ácido salicílico también produce toxicidad sistémica. El ácido salicílico se utiliza en el tratamiento de las infecciones superficiales por hongos, el acné, la psoriasis, la dermatitis seborreica, las verrugas y otras dermatosis por descamación.Cuando se combina con azufre, algunos creen que se produce un efecto queratolítico sinérgico. Las preparaciones comunes incluyen una pomada al 3% y al 6% con igual concentración de azufre; una solución de propilenglicol al 6% (Keralyt); del 5% al 20% con partes iguales de ácido láctico en colodión flexible para las verrugas (Duofilm, Occlusal); en una base de crema a cualquier concentración para efectos queratolíticos; como una pomada al 60% para las verrugas plantares; y en un emplasto al 40% sobre tela de terciopelo para el tratamiento de callos y verrugas (emplasto de ácido salicílico al 40%).
Preparación
Se prepara calentando fenolato de sodio con dióxido de carbono a presión
Métodos de producción
El ácido salicílico se biosintetiza a partir del aminoácido fenilalanina. En Arabidopsis thaliana también puede sintetizarse a través de una vía independiente de la fenilalanina.
El salicilato de sodio se prepara comercialmente tratando el fenolato de sodio (la sal sódica del fenol) con dióxido de carbono a alta presión (100 atm) y alta temperatura (390K) -un método conocido como la reacción de Kolbe-Schmitt. La acidificación del producto con ácido sulfúrico da ácido salicílico :
También puede prepararse mediante la hidrólisis de la aspirina (ácido acetilsalicílico) o del salicilato de metilo (aceite de verde invierno) con un ácido o una base fuertes.
nombre de la marca
Advanced Pain Relief Callus Removers (Schering-Plough HealthCare); Advanced Pain Relief Corn Removers (Schering-Plough HealthCare); Clear Away Wart Remover (Schering-Plough HealthCare); Compound W (Whitehall-Robins); Dr. Scholl’s Callus Removers (Schering-Plough HealthCare); Dr. Scholl’s Corn Removers (Schering-Plough HealthCare); Dr. Scholl’s Wart Remover Kit (Schering-Plough HealthCare); Duofilm Wart Remover (Schering-Plough HealthCare); Duoplant (Stiefel); Freezone (Whitehall-Robins); Ionil (Galderma); Ionil-Plus (Galderma); Salicylic Acid Soap (Stiefel); Saligel (Stiefel); Stri-Dex (Sterling Health U.S.A.).
Referencia(s) de síntesis
The Journal of Organic Chemistry, 27, p. 3551, 1962 DOI: 10.1021/jo01057a035
Tetrahedron Letters, 37, p. 153, 1996 DOI: 10.1016/0040-4039(95)02120-5
Descripción general
Sólido inodoro de color blanco a bronceado claro. Se hunde y se mezcla lentamente con el agua.
Aire & Reacciones con el agua
Se sublima y forma vapor o polvo que puede explotar .
Perfil de reactividad
El ácido salicílico es un ácido carboxílico. Los ácidos carboxílicos donan iones de hidrógeno si hay una base que los acepte. Reaccionan así con todas las bases, tanto orgánicas (por ejemplo, las aminas) como inorgánicas. Sus reacciones con las bases, denominadas «neutralizaciones», van acompañadas de la evolución de importantes cantidades de calor. La neutralización entre un ácido y una base produce agua y una sal. Los ácidos carboxílicos con seis o menos átomos de carbono son libre o moderadamente solubles en agua; los que tienen más de seis carbonos son ligeramente solubles en agua. Los ácidos carboxílicos solubles se disocian en cierta medida en el agua para dar lugar a iones de hidrógeno. Por ello, el pH de las soluciones de ácidos carboxílicos es inferior a 7,0. Muchos ácidos carboxílicos insolubles reaccionan rápidamente con soluciones acuosas que contienen una base química y se disuelven porque la neutralización genera una sal soluble. Los ácidos carboxílicos en solución acuosa y los ácidos carboxílicos líquidos o fundidos pueden reaccionar con metales activos para formar hidrógeno gaseoso y una sal metálica. En principio, estas reacciones también se producen con los ácidos carboxílicos sólidos, pero son lentas si el ácido sólido permanece seco. Incluso los ácidos carboxílicos «insolubles» pueden absorber suficiente agua del aire y disolverse lo suficiente en el ácido salicílico como para corroer o disolver piezas y recipientes de hierro, acero y aluminio. Los ácidos carboxílicos, al igual que otros ácidos, reaccionan con las sales de cianuro para generar cianuro de hidrógeno gaseoso. La reacción es más lenta para los ácidos carboxílicos secos y sólidos. Los ácidos carboxílicos insolubles reaccionan con soluciones de cianuro para provocar la liberación de cianuro de hidrógeno gaseoso. Se generan gases inflamables y/o tóxicos y calor por la reacción de los ácidos carboxílicos con compuestos diazo, ditiocarbamatos, isocianatos, mercaptanos, nitruros y sulfuros. Los ácidos carboxílicos, especialmente en solución acuosa, también reaccionan con sulfitos, nitritos, tiosulfatos (para dar H2S y SO3), ditionitos (SO2), para generar gases inflamables y/o tóxicos y calor. Su reacción con los carbonatos y bicarbonatos genera un gas inofensivo (dióxido de carbono) pero también calor. Al igual que otros compuestos orgánicos, los ácidos carboxílicos pueden ser oxidados por agentes oxidantes fuertes y reducidos por agentes reductores fuertes. Estas reacciones generan calor. Es posible obtener una gran variedad de productos. Al igual que otros ácidos, los ácidos carboxílicos pueden iniciar reacciones de polimerización; al igual que otros ácidos, suelen catalizar (aumentar la velocidad de) reacciones químicas.
Peligro
Alcalosis respiratoria, hipercalemia, hipertermia, deshidratación, convulsiones, shock, parálisis res-piratoria, acidosis respiratoria, lesiones y muerte por colapso respiratorio; fetotóxico.
Peligro para la salud
La inhalación de polvo irrita la nariz y la garganta. Pueden producirse vómitos espontáneos si se ingieren grandes cantidades. El contacto con los ojos provoca irritación, dolor intenso y lesiones en la córnea que deberían curarse. El contacto prolongado o repetido con la piel puede causar una marcada irritación o incluso una leve quemadura.
Mecanismo de acción
Se ha demostrado que el ácido salicílico actúa a través de varias vías diferentes. Produce sus efectos antiinflamatorios mediante la supresión de la actividad de la ciclooxigenasa (COX), una enzima responsable de la producción de mediadores proinflamatorios como las prostaglandinas. En particular, no lo hace mediante la inhibición directa de la COX, a diferencia de la mayoría de los demás antiinflamatorios no esteroideos (AINE), sino mediante la supresión de la expresión de la enzima (a través de un mecanismo aún no dilucidado). También se ha demostrado que el ácido salicílico activa la proteína quinasa activada por el monofosfato de adenosina (AMPK), y se cree que esta acción puede desempeñar un papel en los efectos anticancerígenos del compuesto y de sus productos, la aspirina y el salsalato. Además, es probable que los efectos antidiabéticos del ácido salicílico estén mediados por la activación de la AMPK, principalmente a través de un cambio conformacional alostérico que aumenta los niveles de fosforilación. El ácido salicílico también desacopla la fosforilación oxidativa, lo que conduce a un aumento de las proporciones ADP:ATP y AMP:ATP en la célula. Por lo tanto, el ácido salicílico puede alterar la actividad de la AMPK y, posteriormente, ejercer sus propiedades antidiabéticas a través de la alteración del estado energético de la célula. Sin embargo, incluso en los ratones con AMPK knock-out se produce un efecto antidiabético, lo que demuestra que existe al menos una acción adicional, aún no identificada, del compuesto.
Efectos secundarios
Los efectos secundarios del ácido salicílico incluyen eritema y descamación.
Perfil de seguridad
Es tóxico por ingestión, por vía intravenosa y por vía intraperitoneal. Moderadamente tóxico por vía subcutánea. Un teratógeno experimental. Efectos sistémicos en humanos por contacto con la piel: acúfenos. Se han notificado datos sobre mutaciones. Es un irritante cutáneo y ocular grave. Efectos reproductivos experimentales. Incompatible con sales de hierro, éter nitroso, acetato de plomo, yodo. Se utiliza en la fabricación de aspirina. Cuando se calienta hasta su descomposición, emite un humo acre y vapores irritantes.
Exposición potencial
Se utiliza como agente queratolítico tópico; en la fabricación de aspirina, salicilatos, resinas, como intermedio de colorantes; inhibidor de la prevulcanización; reactivo analítico; fungicida, antiséptico y conservante de alimentos.
Fármacos y tratamientos veterinarios
A menudo combinados con azufre, los champús de ácido salicílico se emplean a menudo para tratar a pacientes con trastornos seborreicos (seborrea sicca andoleosa) que presentan una descamación de leve a moderada, con leves restos cerosos y queratinosos. En concentraciones más altas, los productos tópicos como Kerasolv Gel (ácido salicílico al 6,6%) pueden utilizarse para eliminar el exceso de tejido localizado asociado a los trastornos hiperqueratósicos, como las callosidades y el engrosamiento idiopático del planum nasale y las almohadillas de los pies.
El ácido salicílico tiene acciones ligeramente antipruriginosas, antibacterianas (bacteriostáticas), queratoplásticas y queratolíticas. Las concentraciones más bajas son principalmente queratoplásticas y las más altas, queratolíticas. El ácido salicílico reduce el pH de la piel, aumenta la hidratación de los corneocitos y disuelve el aglutinante intercelular entre los corneocitos. Se cree que el ácido salicílico y el azufre son sinérgicos en sus acciones queratolíticas.
Métodos de purificación
Se ha purificado por destilación al vapor, por recristalización a partir de H2O (la solubilidad es del 0,22% a temperatura ambiente y del 6,7% a 100o), MeOH absoluto o ciclohexano y por sublimación al vacío a 76o. El cloruro de ácido (agujas) tiene m 19-19,5o, b 92o/15mm, la amida tiene m 133o (agujas amarillas de H2O), el derivado O-acetilo tiene m 135o (calentamiento rápido y el líquido se resolidifica a 118o), y el derivado O-benzoilo tiene m 132o (EtOH acuoso). .
Hormona vegetal
El ácido salicílico (SA) es una fitohormona fenólica y se encuentra en las plantas con funciones en el crecimiento y desarrollo de la planta, la fotosíntesis, la transpiración, la captación y el transporte de iones. El SA también induce cambios específicos en la anatomía de las hojas y en la estructura de los cloroplastos. El SA participa en la señalización endógena, mediando en la defensa de las plantas contra los patógenos. Desempeña un papel en la resistencia a los patógenos al inducir la producción de proteínas relacionadas con la patogénesis. Participa en la resistencia sistémica adquirida (SAR), en la que un ataque patógeno en una parte de la planta induce la resistencia en otras partes. La señal también puede trasladarse a las plantas cercanas mediante la conversión del ácido salicílico en el éster volátil, el salicilato de metilo.
Incompatibilidades
Sales de hierro; acetato de plomo; yodo. Forma una mezcla explosiva en el aire.