INTRODUCTION
Les papillomavirus humains (HPV) conforment un groupe viral hétérogène ; leur génome est constitué d’une molécule d’ADN double brin hélicoïdale avec une capside protéique. Ils sont formés d’entités épithéliotropes qui infectent l’état basal de l’épithélium et, par conséquent, préservent la transcription et la réplication de son ADN à des niveaux basaux, produisant des lésions papillomateuses et verruqueuses hyperplasiques dans la peau et les muqueuses.1
Il existe plus de 230 types de HPV (dont 118 bien caractérisés) et plus de 40 types anal-génitaux, dont 15 sont oncogènes. Chez l’homme, ils représentent l’un des groupes viraux infectant le plus fréquemment l’épithélium de la peau et des muqueuses conjonctives, de la cavité buccale (génotypes 33 et 32) du larynx, de l’arbre bronchique, de l’œsophage, de la vessie, de l’anus et des voies génitales.2,3
Dans le cas des HPV de la langue, il existe deux groupes principaux de présentation clinique :
a) les lésions bénignes et b) les lésions pré-malignes ou malignes. Parmi les lésions buccales bénignes, nous pouvons trouver le papillome buccal, la verrue buccale vulgaire (verrue commune), le condylome acuminé buccal et l’hyperplasie épithéliale focale (maladie de Hecks).4-6 Les lésions malignes et pré-malignes sont principalement représentées par la leucoplasie et le carcinome épidermoïde7.
Le papillome squameux de la muqueuse buccale est la lésion papillaire la plus fréquemment rencontrée, il représente 2,5 % ou toutes les lésions trouvées dans la bouche.6 Les lésions cliniques du HPV sont le plus souvent observées sur la lèvre supérieure, la lèvre inférieure, le frein lingual, le dos de la langue et les coins des lèvres8.
La morphologie la plus couramment observée de ces lésions assume une forme de chou-fleur, néanmoins, d’autres formes peuvent être observées comme des verrues communes, des hyperkératoses ou même des surfaces non kératinisées, qui présentent des changements de couleur superficiels (normalement une teinte violette).9 Selon les références bibliographiques, cette maladie est principalement transmise par une pratique sexuelle bucco-génitale10.
Le but de la présente étude était de réaliser une revue de la littérature sur la revue de la papillomatose orale ainsi que de rapporter un cas clinique.
HISTOLOGIE DE LA LANGUE
Les cellules situées dans la langue présentent un arrangement structural polystratifié. Elles sont installées sur un stratum corneum (superficiel), une couche granuleuse, une couche épineuse et une couche basale (couche la plus profonde). Le noyau de ces cellules change de taille en fonction de leur maturité et de leur spécialisation.11
PAPILLOMA VIRUS GENOME
Les particules virales sont composées d’une capside protéique qui est composée de 95% de protéine L1 et de 5% de protéine L2. Ces protéines se lient pour former des capsomères icosaédriques. Un ADN circulaire double brin d’environ 8000 paires de bases se trouve à l’intérieur de la capside. Elle est formée de huit gènes et d’une région régulatrice non codifiée ; cette région contient des sites de liaison pour les facteurs hormonaux et protéiques de l’hôte, dont le virus a besoin pour achever son cycle de réplication.12
Le virus du VPH est pareillement conformé par deux types de gènes : les gènes codifiés pendant les stades précoces de l’infection, plus connus sous le nom de gènes E (E pour early) et les gènes codifiés pendant les stades tardifs de la réplication connus : E1, E2, E4, E5, E6, E7 (bien que E4 soit considéré comme un gène tardif) ainsi que deux gènes tardifs, L1 et L2. Les gènes précoces codifient des protéines impliquées dans la réplication et la régulation virale, ainsi que dans leur capacité cancérigène. En revanche, les gènes tardifs codifient des protéines structurelles qui forment une capside virale.12,13
CYCLE DE VIE DU VPH
Le VPH pénètre dans l’hôte par une petite abrasion de l’épithélium intégral de la langue.13 Il entame alors son cycle productif en infectant les cellules peu différenciées des couches basales de l’épithélium, où la transcription des gènes commence12.
Lorsque les cellules infectées se différencient et migrent de la couche basale vers la couche épineuse de l’épithélium (permissibilité immunologique), la réplication virale est stimulée produisant ainsi l’accumulation des virions au sein du noyau et l’assemblage de la capside dans le cytoplasme. Il existe au moins deux cycles de réplication virale : a) l’infection lytique et b) l’infection lysogène.
En cas d’infection lytique, le virus arrive dans les cellules para-basales avec une capacité de réplication, il pénètre dans le cytoplasme puis dans le noyau. Une fois dans le noyau, il se réplique dans la zone épisomale, sans s’intégrer au génome cellulaire, produisant ainsi environ 20 copies virales. Ces particules virales complètes provoquent la mort cellulaire et restent donc libres et à proximité des surfaces épithéliales.
En cas d’infection lysogène, le génome cellulaire est directement affecté. C’est le cas des HPV à haut risque (16 et 18). Après avoir atteint le noyau cellulaire, le virus s’intègre dans le génome cellulaire de l’hôte, principalement les segments E6 et E7. Dans ce cas, la réplication du virus passe par un stade de latence jusqu’à ce que la cellule hôte réplique son propre ADN ainsi que l’ADN des virus intégrés. Les segments d’ADN viraux sont transcriptionnellement actifs après la division cellulaire ; cela garantit leur propagation13 Contrairement aux cas d’infection lytique, ce type d’infection est observé dans les cellules connaissant une croissance maligne.
L’expression génétique des différents types de HPV est strictement et spécifiquement régulée par des facteurs de transcription tels qu’un AP-1, un facteur spécifique aux kératinocytes, NF-1CTF, CEFI, CEFII et TEFI ainsi que certains facteurs d’origine hormonale.
Dans les deux types d’infection, les protéines E1 et E2 initient leur expression dans un sens ascendant (suprarégulation), activant ainsi la transcription de l’ADN ainsi que l’expression contrôlée des cellules basales12.
Les gènes HPV E6 et E7 sont directement liés à la transformation maligne des cellules par le biais des oncoprotéines E6 et E7. Ces protéines sont capables de former des composés avec des produits génétiques cellulaires qui régulent le cycle cellulaire, parmi lesquels on trouve p53 et Rb. L’oncoprotéine E6 crée un composé avec la protéine p53, tandis que E7 crée un composé avec la protéine Rb.
La protéine Rb régule le passage de G1 à S L’oncoprotéine E7 séquestre Rb l’empêchant de réguler les protéines de la prolifération cellulaire, cela oblige le cycle cellulaire à rester en phase de synthèse.13 Ces deux événements : intégration du gène viral au génome cellulaire et blocage de la fonction normale des gènes suppresseurs de tumeurs p53 et Rb sont associés à la transformation cellulaire des cellules infectées par des virus à fort potentiel oncogène (16 et 18). Les changements progressifs subis par les kératocytes modifient le microenvironnement et altèrent l’équilibre de l’épithélium bien que les stimuli de prolifération cellulaire soient guidés par la sécrétion de facteurs de croissance épidermique alpha et bêta.
Les protéines E2, E3, E4, E5, E6 et E7 induisent une perte de contrôle des protéines du gène (ADN épisomal au centre du noyau) tandis que E6 et E7 répliquent l’ADN viral. L1 et L2 assemblent le virus et se placent dans les cellules malpighiennes matures pour s’en débarrasser ultérieurement (plus de 1 000 copies par cellule).
Dans les lésions bénignes, comme le papillome de la langue, la prolifération des particules d’ADN épisomal favorise une croissance anormale de l’épithélium, augmentant ainsi les erreurs génétiques des cellules (gastogenèse).
E6 et E7 favorisent la prolifération du virus et son immortalisation. Lorsque le virus possède un potentiel oncogène, il provoque une malignisation, lorsqu’il n’en possède pas, il se développe une lésion bénigne qui peut s’auto-limiter en deux ans. Ce mécanisme est principalement induit par la perte des télomères de l’ADN, qui inhibe l’apoptose, augmente le nombre de cellules infectées et diminue l’acétylation et la phosphorylation de p53 et Rb. De plus, l’expression des facteurs angiogéniques est favorisée. C’est le cas du facteur de croissance vasculaire qui désorganise le cytosquelette cellulaire et la matrice extracellulaire affectant les facteurs de régulation qui participent à la santé de ces structures.12
L’infection par le VPH provoque d’importants changements dans la morphologie cellulaire. Par exemple, on observe la formation de vacuoles péri-nucléaires, des noyaux élargis, irréguliers et hyperchromatiques ainsi qu’une bi-nucléation. Les cellules qui ont subi ces changements sont appelées koylocytes et sont considérées comme » l’empreinte digitale » du virus.
Le condylome est la manifestation morphologique la plus courante de l’infection par le VPH (condylome acuminé).14
PRÉSENTATION DU CAS
La patiente était une femme célibataire de 21 ans. Elle ne travaillait pas en dehors de son domicile, était née et résidait dans l’Estado de Mexico (État du Mexique). Son groupe sanguin était O, Rh positif. Dans le cadre de ses antécédents familiaux, elle a déclaré que son père était atteint de sclérose en plaques et que sa sœur souffrait de polyarthrite rhumatoïde. La patiente a nié toute toxicomanie. Elle souffrait de multiples fibroadénomes juvéniles au sein gauche, qui ont été traités chirurgicalement. Elle a commencé à avoir des règles à 15 ans, avec un rythme menstruel de 28 × 3. L’activité sexuelle a débuté à 17 ans. Elle a déclaré avoir eu un partenaire sexuellement actif et a nié avoir eu des rapports sexuels oraux et génitaux. Elle a connu une grossesse et a été mise au monde d’un enfant vivant de 3,1 kg.
Un an auparavant, elle avait été soumise à des études de cytologie et de colposcopie dans le tractus génital inférieur, en plus d’un examen des seins. Les résultats se sont révélés négatifs pour le cancer et le VPH. La méthode de planification familiale utilisée par la patiente était le dispositif intra-utérin.
La patiente a consulté pour la première fois en avril 2014, se plaignant d’une glossodynie ventrale avec une évolution de trois mois. Après cela, elle a ressenti une sensation de corps étranger et de bombement dans les tissus mous, avec une croissance centrifuge progressive jusqu’à la formation d’une tumeur en forme de lentille qui saignait au contact du palais dur et pendant la mastication. Elle a consulté un cabinet médical où elle a reçu un traitement systémique non spécifié qui n’a pas donné de résultats satisfaisants.
La bouche a été inspectée par une procédure de colposcopie avec un grossissement de 0,66x (colposcope Hinselmann, Mexique 2014). Ladite procédure a révélé une lésion d’environ 1cm de diamètre, de teinte rosée, de forme circulaire, aux bords déchiquetés, sans pédicule et de nature avasculaire (Figure 1). Une fois l’étude terminée, le patient a été informé du diagnostic et du traitement souhaitable.
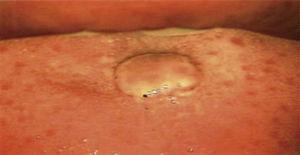
Inspection directe de la bouche sous perspective colposcopique. I (Hinselmann, 2014), avec un grossissement de 0,66. Lésion mesurant 1cm de diamètre, de teinte rosée, de forme circulaire, aux bords déchiquetés, avasculaire et sans pédicule.
TREATMENT
Sous anesthésie locale et xylocaïne à 2% avec épinéphrine (1mL) la base de la lésion a été infiltrée avec une aiguille de calibre 30G. La surface de la lésion a été clippée et disséquée en entreprenant une dissection cunéiforme. Après hémostase, les bords ont été recouverts (Dermalon 000) dans un plan avec des sutures inversées. Le spécimen obtenu a été fixé dans 5ml de formol à 10% pour être ensuite envoyé au service de pathologie.
Quinze jours plus tard, les sutures ont été retirées et une zone chirurgicale saine a ainsi été obtenue (Figure 2). Le rapport histopathologique a révélé la présence d’un tissu de 0,6 × 0,5cm de dimensions. Le spécimen était de forme irrégulière, de teinte brun foncé et de consistance molle. L’analyse au microscope a révélé un épithélium cornéen poly-stratifié, une acanthose et une hyperkératose. L’intérieur de l’échantillon a révélé des foyers de cornification intra-épithéliale de différentes tailles. En général, les cellules épithéliales étaient de plus petite taille que celles du stratum spinosum normal (Figures 3 et 4). Le diagnostic final a indiqué un papillome squameux de la langue. Le typage génétique viral réalisé par réaction en chaîne par polymérase (PCR) en temps réel rapportait la présence d’un génotype 58 (virus à haut risque).
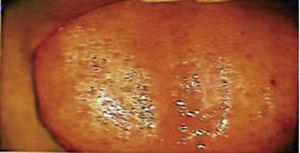
Photographie de la langue sous perspective colposcopique 15 jours après la chirurgie.
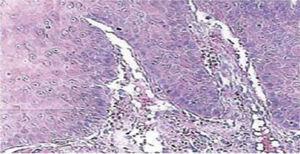
Agrandissement microscopique 10x. Epithélium cornéen poly-stratifié, acanthose et hyperkératose.
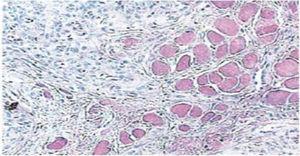
40 x Agrandissement microscopique. Foyers de cornification intra-épithéliale de différentes tailles.
DISCUSSION
Le VPH est un virus à ADN ; il appartient à la famille des papovaviridae, du genre papillomavirus. Plus de 230 génotypes ont été décrits. La période d’incubation varie de trois semaines à huit mois, avec une moyenne de trois mois. Sur les 230 génotypes de papillomavirus, 16 sont le plus souvent associés à des lésions buccales (1, 2, 3, 4, 6, 7, 10, 11, 13, 16, 31, 32, 33, 35 et 57).
Il existe deux grands groupes de présentation clinique du HPV : a) les lésions bénignes et b) les lésions prémalignes ou malignes. Les lésions buccales bénignes comprennent le papillome buccal, la verrue vulgaire (verrue commune), le condylome acuminatum buccal et l’hyperplasie épithéliale focale (maladie de Heck). Les lésions prémalignes et malignes sont principalement représentées par la leucoplasie et le carcinome épidermoïde associés aux génotypes 16 et 18. La transmission du HPV se fait par les pratiques sexuelles orales-génitales.
Il existe plusieurs techniques pour diagnostiquer le HPV, parmi elles nous pouvons compter la cytologie conventionnelle, la cytologie à base liquide, l’histologie, la colposcopie et les techniques de biologie moléculaire telles que l’hybridation in situ et la réaction en chaîne par polymérase (PCR).15,16 Dans le cas clinique ici présenté, il a été décidé d’entreprendre un typage génétique du virus par PCR, cette procédure a révélé la présence d’un génotype 58. Cette donnée n’a pas été documentée dans la classification rapportée dans la littérature.
Le traitement est adapté à chaque cas particulier. Des techniques destructrices peuvent être utilisées, comme la cryothérapie ou l’électrochirurgie, l’utilisation d’immunémodulateurs (imiquimod à 5%), ou l’utilisation d’un antimétabolite pour interférer avec l’ARN (acide ribo-nucléique) et l’ADN, ou par l’inhibition de la thymidylate synthétase (5-fluororacil).17,18 Dans le cas présent, il a été décidé d’utiliser la chirurgie au bistouri froid en fonction du site d’apparition de la lésion, pour se prévaloir de la possibilité de ne pas laisser de séquelles.
CONCLUSION
Dans la muqueuse buccale exposée à des microtraumatismes, les micro-organismes ainsi que les facteurs chimiques et physiques peuvent agir en synergie avec le HPV pour favoriser le développement de lésions bénignes ou de carcinomes.
Le HPV joue un rôle important dans le développement du carcinome épidermoïde dans les voies anales et génitales ainsi que dans l’épidermodysplasie verruciforme, et dans le larynx.
Dans les lésions bénignes, les génotypes 33 et 32 sont les plus fréquents. Néanmoins, dans notre étude, le rapport de la procédure de biologie moléculaire a indiqué la présence du génotype 58.
Dans la littérature mondiale, le génotypage 58 n’a pas été rapporté dans ce type de lésions qui, cliniquement, semblent présenter un comportement bénin.
Pour aborder avec succès cette affection, un diagnostic et un traitement interdisciplinaires entre dentistes, oncologues et gynécologues convenablement formés à l’étude de ces lésions sous la perspective colposcopique sont de la plus haute importance.
Le traitement exécuté par une intervention chirurgicale au bistouri froid, visant à laisser des frontières sans lésions est une solution adéquate pour éradiquer ce type de lésions et ne causer aucune séquelle, surtout dans les tumeurs qui semblent être cliniquement bénignes, mais qui selon leur type de gène, subiront un comportement malin à moyen et long terme.
Nous considérons que le présent rapport de cas est intéressant car il y avait peu de rapports liés à cette condition dans la bibliographie scientifique mexicaine.